ミニ特集「身体の情報処理がこころをつくる」:意思決定を創発する脳と身体の情報処理
心理・認知科学専攻 大平英樹
はじめに
あなたが、昼食に何を食べるか迷っている場面を想像して下さい。行きつけのラーメン屋は、こってり系の豚骨スープが実に旨い。でも最近開店したエスニック料理の店も気になる…。心理学では、こうした、価値に基づく選択を意思決定(decision-making)と呼びます。あの店のラーメンにはいつも満足しましたが(高い価値)、通い過ぎて少し飽きてきた気もします(価値低減)。エスニック料理店に行ってみたいけど、値段が高い割に美味しくなかったらどうしよう(価値の不確実性)。私たちの日常生活は、こうした意思決定の連続です。おそらく私たちの脳が、何らかの原理によって、膨大な情報処理に基づいて意思決定を実現していると考えることができます。
今日はラーメン屋にしようと決めたなら、昼休み時間になったら、すぐに出かけねばなりません。あの店にはいつも行列ができるから…。意思決定は、望ましいもの(報酬)を獲得したり、望ましくないもの(損失)を避けたりするために行うので、多くの場合身体の運動を伴います。この時あなたの脳は、ラーメン屋まで急いで歩くためには、身体を動かす資源が必要だと予測します。その結果、オフィスを出る頃には、あなたの心拍や血圧は上がり、糖を骨格筋に効率的に分配するための準備ができていることでしょう。こうした仕組みを心理学者のバレットは、「身体予算(body budget)の管理」と名付けました(2021)。家計や国家財政では、稼いだり使ったりした予算が監視され制御されます。同じように身体予算の管理では、水分、塩分、糖などの身体資源が監視され、運動したり頭を使ったりという活動をするごとに身体口座から預金が引き出されます。また食事をしたり、睡眠を取ったりすることで、預金を増やせます。家計や国家財政と同様、もし行き当たりばったりの管理をしたならば、たちまち身体予算は危機に瀕するでしょう。そこで脳は、現在の身体予算を正確に把握しながら、先を読んだ予測によりその使途を制御しようとします。このメカニズムを、アロスタシス(allostasis:変化による恒常性維持の意味)と呼びます。
私の研究室では、こうした意思決定に伴う脳と身体の活動を調べ、意思決定を効率的に実現するアロスタシスのメカニズムを解明することを目指しています。
意思決定に伴う身体状態の制御
私たちは、意思決定に伴う脳活動、自律神経系・内分泌系・免疫系などの生理的反応の挙動を、シンプルなギャンブル課題を用いて検討してきました(Kimura, et al, 2007; Ohira, et al, 2009; Ohira, et al, 2010)。実験参加者は、図1Aのような2つの選択肢から1つを選びます。その結果として、ある確率で金銭的な報酬が得られたり、損失を被ったりします。
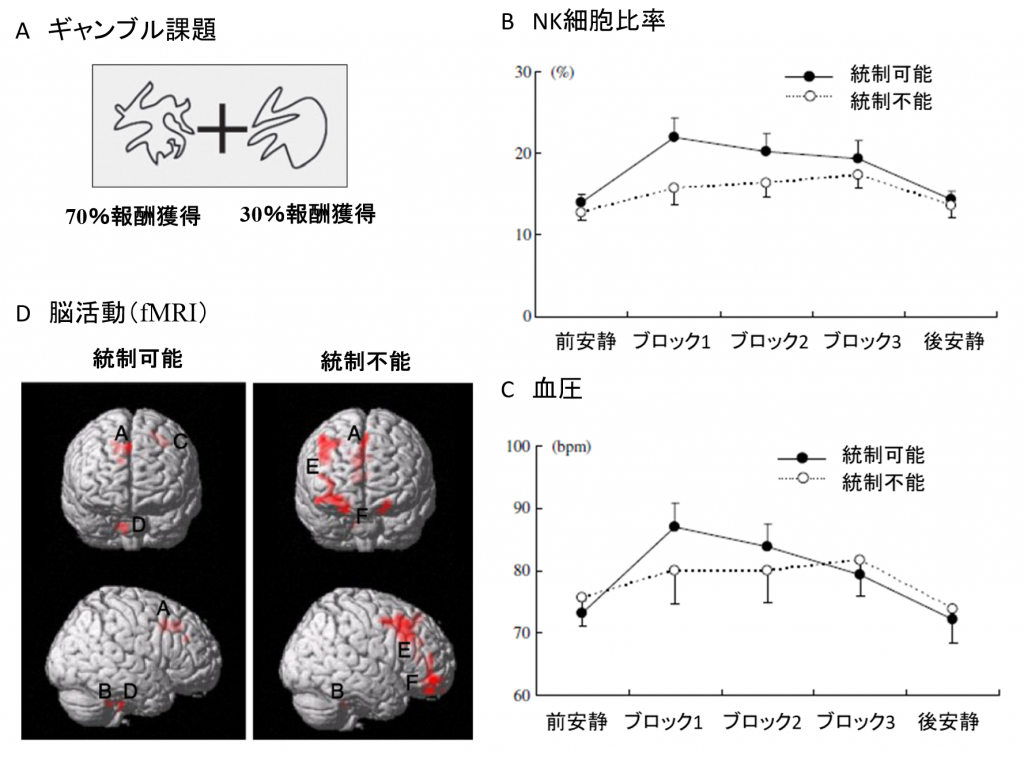
A:ギャンブル課題。参加者は、提示された2つの無意味な図形から1つを選択する。図形ごとに決まった確率で金銭的報酬が与えられる。B:課題中のNK細胞の反応。C:課題中の血圧の反応。D:課題中の脳活動(図中A:前部帯状皮質、B:小脳、E:外側前頭前皮質、F:前頭眼窩皮質)。
私たちの研究では、一方の選択肢が70%,他方が30%で報酬をもたらす条件(統制可能条件)と、参加者の選択とは無関係にランダムに報酬が与えられる条件(統制不能条件)が設けられました。これは、統制可能性(controllability)と 呼ばれ、心理学の意思決定研究ではよく検討されてきた要因です。一般に統制可能な状態の方が満足感などの快の感情が強く経験されます。一方、結果的に獲得した金額が 同じであっても統制不能な状態に置かれるとストレス感が経験されると言われており、これはうつ病の行動的モデルとも考えられています。
統制可能条件では、免疫系反応(血液中リンパ球におけるナチュラル・キラー(natural killer: NK)細胞 の比率:図1B)にも自律神経系反応(血圧(図1C))にも、課題開始と共に強い反応が生じ、課題の進行につれてその反応は馴化していくという一貫した傾向が見られました。これに対して統制不能条件では、いずれの生理的指標においても反応は顕著に抑制されていました。この結果からすぐ思いつくのは、統制不能な状態では参加者はやる気を無くし、学習の努力を放棄してしまったという可能性です。もしそうならば、身体予算がカットされ、それにより生理的反応が低下したのだと解釈できるでしょう。しかし脳活動を調べると、むしろ統制不能条件の方が、前部帯状皮質(anterior cingulate cortex)や前頭眼窩皮質(orbitofrontal cortex)などの、意思決定・学習・価値の評価などに関わりが深いとされている脳部位の活動が強いことがわかりました(図1D)。ここから、統制不能な状態に置かれた参加者は、単にやる気を失って適当な選択をしたわけではなく、課題中を通じて報酬を得る努力を継続していたことが伺えました。
そこで私たちは、脳が自身の意思決定の状態を評価し、それにより身体の活動状態を制御したのではないかと考え、その可能性を検証しようと試みました。脳が身体を制御するための情報伝達経路としては、自律神経系とホルモンを用いる液性の経路があります。私たちは、このうち最も反応性が早く、情報伝達効率がよいと考えられる迷走神経系(vagus nervous system)に注目しました。迷走神経系は副交感神経系を構成する代表的な神経系であり、単純に言うと、この神経系の活動が高まると身体活動にブレーキがかかり、心拍や血圧が低下すると考えることができます。私たちの心臓の拍動間隔は1拍ごとに変化していますが、これを心拍変動性と呼び、迷走神経系活動のよい指標になることがわかっています。実験データの解析から、統制不能な条件では、課題中の心拍変動性が顕著に高まることが示され、しかもその度合いは、前部帯状皮質や外側前頭前皮質などの意思決定や実行機能に関連が深い脳部位の活動と相関していることが分かりました。つまり脳は、自分自身の選択とその結果生じる報酬の獲得との関係(これを随伴性(contingency)と呼びます)を監視し、その結果現在の状態が統制不能であると評価されると、積極的に身体の活動状態を抑制する方向に制御していたのではないかと考えることができます。これはおそらく、統制不能な状態では近い将来どういう事態になるかの予測が困難であり、そこでやみくもに身体予算を浪費するのは危険であるため、身体予算を節約しておこうという目的からではないかと推測されます。
迷走神経系:脳と身体を繋ぐ情報ハイウェイ
自然環境でも社会環境でも、選択と結果の随伴性は固定されているわけではなく、時間と共に変動します。行きつけのラーメン屋が、経営者が変わったり、コスト・カットのために材料を節約したりして、いつの間にか味が落ちてしまうということもあるでしょう。そのような場合にはラーメン屋に行く回数を減らし、他の店を試した方が満足感を高めることができそうです。このように私たちは、環境への適応のために随伴性の変化に鋭敏に追従して自らの行動を変えていく必要があります。
身体予算の考え方からは、随伴性の変化に応じて生理的反応が柔軟に調整されるだろうと予測されます。Smithら(2017)は、ここでも心拍変動性が、脳が随伴性の変化に応じて身体活動を調整していく機能の指標になると論じています。上に述べたように心拍変動性は迷走神経の働きを示す指標であり、脳が迷走神経系を介して、身体のさまざまな活動をトップ・ダウン的に制御する機能を反映すると考えられているのです(Thayer, et al. 2012)。もしそうならば、心拍変動性の高い人は、随伴性の変化により敏感に気づき、それによって、より効率的に自分の身体活動を調整していくことができるだろうと想像されます。
私たちは(Ohira, et al. 2013)、はこの仮説を検討するために、心拍変動性が高い群と低い群の参加者に、先ほどと同様なギャンブル課題をしてもらいました。この研究では、有利・不利な選択肢が課題途中で突然逆転され、そのため参加者はそれまで学習した行動を抑制し、新たな随伴性を再学習することを迫られました。これを逆転学習(reversal learning)と呼びます。心拍変動性が高い群は、随伴性の逆転の導入に伴い、自律神経系・内分泌系・免疫系の指標が一貫して高い反応を示しました(図2A)。さらに、意思決定において重要な前部帯状皮質、前頭眼窩皮質、線条体、そして身体と脳を繋ぐインターフェイスであると考えられている島(とう:insula)と呼ばれる脳部位の活動が、それらの生理的反応と強い相関を示しました(図2B)。これに対して心拍変動性が低い群は、脳でも生理的指標でも、随伴性の逆転に伴う反応はほとんど観測されませんでした。この群は随伴性の変化に鈍感であり、随伴性が変化した後でも、それまでに獲得した習慣的な脳と身体の活動パターンが持続されたのだと解釈することができます。もちろん、心拍変動性の高い人たちの方が、行動的にも生理的にも、変化する環境への適応力が高いだろうと考えることができます。
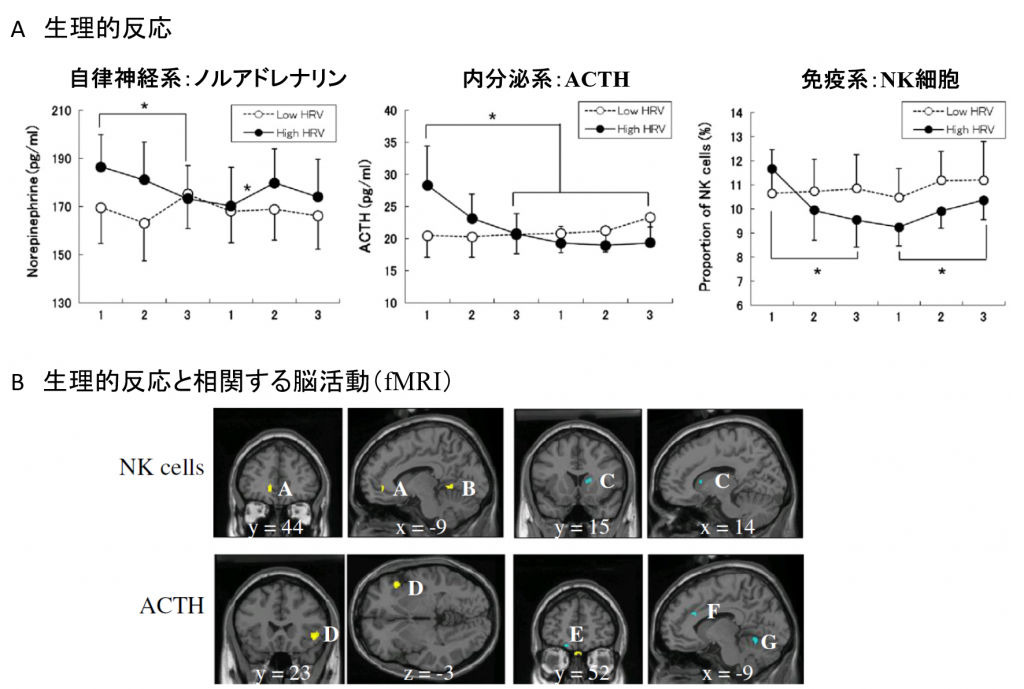
A:逆転学習課題における自律神経系(血中ノルアドレナリン濃度)・内分泌系(血中ACTH濃度)・免疫系(NK細胞比率)の反応。B:生理的反応(ACTH, NK細胞)と相関する脳活動(図中A:前部帯状皮質1、B:小脳、C:線条体、D:島、E:前頭眼窩皮質、F:前部帯状皮質2、G:小脳)。
ここでは脳が身体を制御する遠心性の迷走神経系だけについて述べましたが、逆に身体の状態に関する情報を脳へ伝える求心性の迷走神経系も存在します。迷走神経系は、脳が身体の状態を知り、それをリアルタイムで適切に制御するために、膨大な情報の輸送を担う「情報ハイウェイ」とも言うべきシステムであると言えます。
内受容感覚と意思決定:予測に基づく身体のモニタリングと制御
ここまで述べたように、私たちは意思決定に伴う脳と身体活動を長年研究し、さまざまな興味深い事実を発見してきました。しかし、その背後にあるメカニズムを具体的に説明することは困難でした。
ところが最近になって、こうした問題を考える上で有力な手掛かりが登場しました。それがフリストン(Friston, 2010)により主張されている、予測符号化(predictive coding)、あるいは自由エネルギー原理(free energy principle)と呼ばれる理論です。この理論では、脳は、将来入力される刺激を予測する内的モデルを構築し、その予測と入力された感覚信号の差異(予測誤差:prediction error)の計算に基づいて、知覚を能動的に創発していると主張されます。そして脳は、予測誤差を最小化することにより、自己や世界の安定した像を形成していると考えられています。
ここで重要なのは、身体内部の感覚である内受容感覚(interoception)も、同じような予測的処理により成立していると主張されていることです(Seth & Friston, 2016)。ここでは、内受容感覚は単に受動的に身体の状態を知ることではなく、恒常性を維持して生命を保つために、脳内の内的モデルによる予測と身体信号との差、つまり身体状態の予測誤差を検出し、それを縮小することで身体活動を制御する能動的な過程だと考えられています。さらにKeramatiたち(2014)は、この考え方を拡張し、意思決定に伴う身体活動の制御の過程を説明しようとしています。すなわち、身体状態の予測誤差が生じた際、ある行動を選択することで身体状態が予測に近づけば、それが報酬となりその行動の価値は上がります。意思決定は、そうした身体状態を基盤にした価値に基づく行動の選択として捉えることができます。一方、行動が予測する価値と選択の結果得られた状態の差異、つまり報酬予測誤差が生じる際には、対処のためにエネルギーを高めるべく身体状態の予測が上方修正される。これが先に述べたアロスタシスの機能に対応します。
これは、冒頭に挙げた昼食の選択を思い出すと理解しやすいでしょう。お昼近くになり血糖値や血圧が下がってくると、望ましい血糖値や血圧の予測との間に予測誤差が生じ、私たちはそれを縮めることのできる行動、つまりお店に行って食事することを動機づけられます。それを実行した結果、血糖値や血圧が望ましい値に回復したならば、その店の価値は上がり、近い将来またそこに行く可能性は高まるでしょう。ところが、ラーメン屋を選択して行ってみると長蛇の列ができており、午後の始業開始時間に間に合わないことがわかったとします。この時、美味しいラーメンという報酬を予測したのに、それが裏切られ、負の報酬予測誤差が生じます。すると、空腹を抱えながらも別の店まで歩行移動するために、脳は身体活動のレベルを引き上げます。
この理論は、意思決定と身体予算の管理をうまく説明できるのですが、これまでのところ、全くの仮説でした。しかし最近になり、この考え方を支持する証拠が得られつつあります。例えばLivnehら(2020)は、マウスの島におけるニューロン活動の計測データを機械学習により解析してこの問題を検討しています。島は、身体からの全ての信号が最終的に投射される脳部位であり、内受容感覚の重要な中枢であると考えられています。マウスの島ニューロンは、普段は現在の餓え・渇きの状態を反映する活動パターンを示します。ところが飢餓あるいは渇水状態のときに食物あるいは水を連想する手がかり刺激を提示すると、それらを摂取して満足した状態の活動パターンに変化することが示されました。この時点では、まだ餓えや渇きが癒えてはいないことに注意しましょう。島のニューロンは、いわばそれらの状態を予測するように活動すると考えらます。さらに、こうした機能は、生存に必要な餌や水を摂取するための行動を動機づけると考えられます。
私は、これらの過程を表現する計算論モデルを試作しています(図3A:大平, 2019)。ここでは身体状態として血圧を例に取っています。こうした計算論モデルの利点は、直接観測できない身体状態の予測誤差、報酬予測誤差、などの変化を時系列的に推定し観察できることです。このモデルによりシミュレーションを行うと、統制可能な意思決定課題においては、血圧は課題開始と共に急上昇しますが、学習の進行と共に馴化することが示されました。一方、ランダムに報酬が与えられる統制不能な条件では、血圧は馴化を示さず、徐々に上昇しました(図3B)。それらの結果は、図1Cに示した実際の実験データをよく再現しています。ここで示したのはあくまで定性的で予備的なトイ・モデルであり、その妥当性は今後詳しく検討せねばなりません。しかし、このシミュレーションの結果は、予測に基づく身体のモニタリングと制御というシンプルなメカニズムが、私たち人間が意思決定を行い環境に働きかけ、生命を維持し適応的に生きていく複雑な営みを、創発できる可能性を示しているように思います。
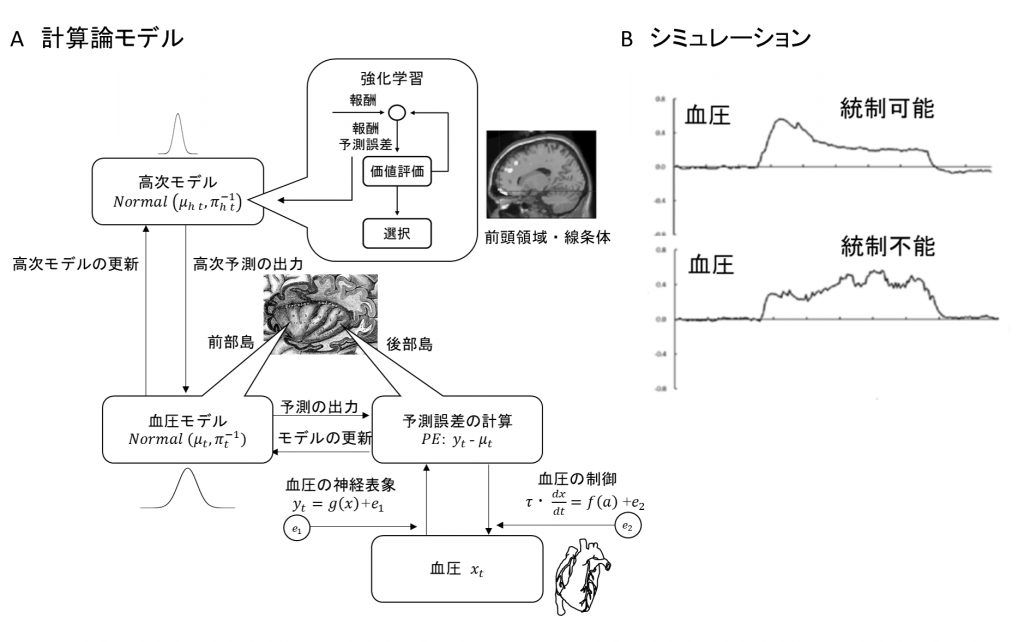
A:意思決定に伴う脳と身体の活動を表現する計算論モデル。B:モデルによるシミュレーション
おわりに
読者の皆さんはこの記事を読んで、ある種の違和感を覚えたかもしれません。それはおそらく、私たちはさまざまな選択を、熟慮した意志によって行っていると思っているのに、この記事では意思決定はあたかも脳や身体が主役であるかのように描かれているためではないでしょうか?
私たちは確かに意識を持っていますし、意思決定もまさに意志によって行っているという強い実感があります。しかしそうした主観的な意識や意志を科学的に研究することには、まだまだ多くの困難があります。そこで私たちは、意識や意志などの主観的な現象をいったん排除し、人間を可能な限り脳や身体という物質に還元し、そこでの情報処理からどのように行動や生理的状態の挙動が創発されるのか、という観点から研究を行っています。この考え方がどこまで正しいかはまだわかりませんが、人間という不思議な存在を理解する1つのあり方ではないか、と考えています。
引用文献
リサ・フェルドマン・バレット (2021). (高橋洋 訳) バレット博士の脳科学教室7 1/2章 紀伊国屋書店.
Friston, K. (2010). The free-energy principle: a unified brain theory? Nature Review Neuroscience, 11, 127-138.
Keramati, M., & Gutkin, B. (2014). Homeostatic reinforcement learning for integrating reward collection and physiological stability. eLife, 3, e04811. doi: 10.7554/eLife.04811.
Kimura, K., Ohira, H., Isowa, T., Matsunaga, M., & Murashima, S. (2007). Regulation of lymphocytes redistribution via autonomic nervous activity during stochastic learning. Brain, Behavior, and Immunity, 21, 921-934.
Livneh, Y., Sugden, A. U., Madara, J. C., Rachel A. Essner, R. A., Flores, V. I., Sugden, L. A., Resch, J. M., Lowell, B. B., & Andermann, M. L. (2020). Estimation of current and future physiological states in insular cortex. Neuron, 105, 1094–1111.
大平英樹 (2019). 脳と身体の予測的符号化とその不全―守谷・国里・杉浦論文へのコメント― 心理学評論, 62, 132-141.
Ohira, H., Fukuyama, S., Kimura, K., Nomura, M., Isowa, T., Ichikawa, N., Matsunaga, M., Shinoda, J., & Yamada, (2009). J. Regulation of natural killer cell redistribution by prefrontal cortex during stochastic learning. NeuroImage, 47, 897-907.
Ohira, H., Ichikawa, N., Nomura, M., Isowa, T., Kimura, K., Kanayama, N., Fukuyama, S., Shinoda, J., & Yamada, J. (2010). Brain and autonomic association accompanying stochastic decision-making. NeuroImage, 49, 1024-1037.
Ohira, H., Matsunaga, M., Osumi, T., Fukuyama, S., Shinoda, J., Yamada, J., & Gidron, Y. (2013). Vagal nerve activity as a moderator of brain–immune relationships. Journal of Neuroimmunology, 260, 28-36.
Seth, A., & Friston, K. J. (2016). Active interoceptive inference and the emotional brain. Philosophical transactions of the royal society B, 371, 20160007.
Smith, R., Thayer, J. F., Khalsa, S. S., & Lane, R. D. (2017). The hierarchical basis of neurovisceral integration. Neuroscience and Biobehavioral Reviews, 75, 274–296.
Thayer, J., Ahs, F., Fredrikson, M., Sollers, J. J., & Wager, T. D. (2012). A meta-analysis of heart rate variability and neuroimaging studies: Implications for heart rate variability as a marker of stress and health. Neuroscience and Biobehavioral Review, 36, 747-756.

